Consiguen revertir las placas del alzhéimer en ratones tras restaurar la barrera hematoencefálica
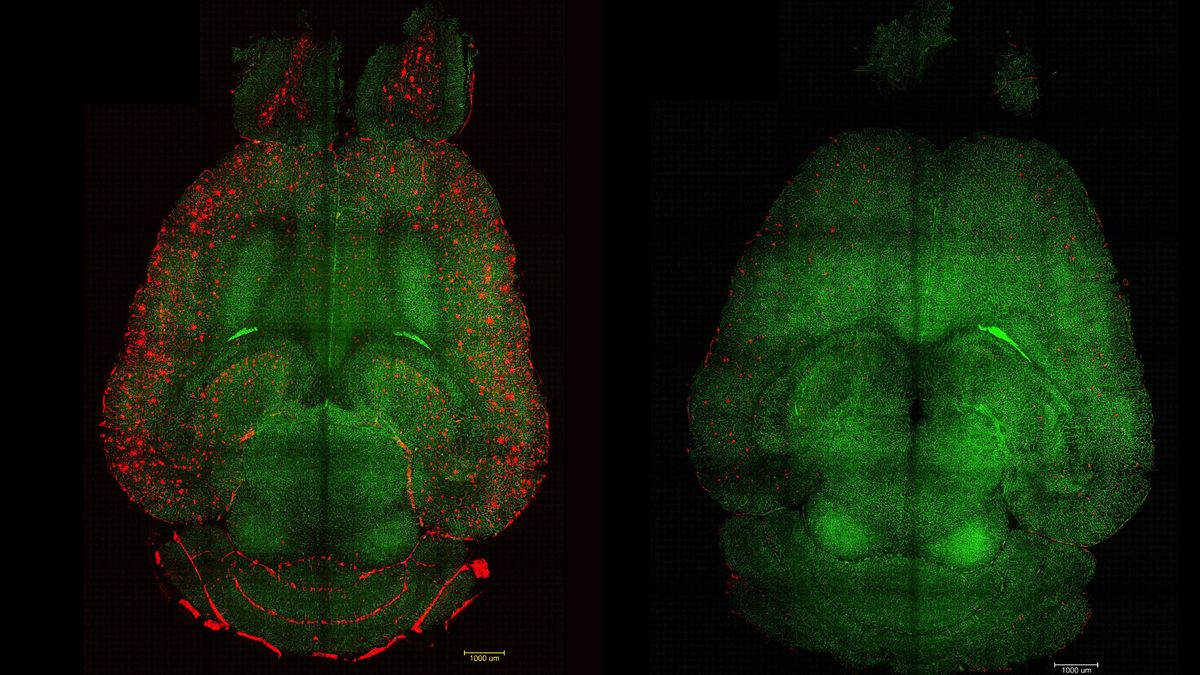
Un equipo de investigación con participación española ha desarrollado una estrategia nanotecnológica que revierte en el cerebro de los ratones las placas de proteínas como las que producen la enfermedad de Alzheimer. Lo que marca la diferencia es que, en lugar de dirigirse directamente a las neuronas, la terapia restaura la función adecuada de la barrera hematoencefálica, el guardián vascular que regula el entorno del cerebro. Al reparar esta interfaz crítica, los investigadores lograron revertir la patología del alzhéimer en modelos animales.
La investigación, que se publica en la revista Signal Transduction and Targeted Therapy, también se diferencia de la nanomedicina tradicional, que se basa en nanopartículas como portadoras de moléculas terapéuticas, y emplea nanopartículas que son bioactivas por sí mismas: “fármacos supramoleculares”.
La barrera hematoencefálica es una barrera celular y fisiológica que separa el cerebro del flujo sanguíneo para protegerlo de peligros externos como patógenos o toxinas. El equipo demostró que la acción sobre un mecanismo específico permite que las proteínas de desecho indeseables producidas en el cerebro atraviesen esta barrera y se eliminen en el flujo sanguíneo. En la enfermedad de Alzheimer, la principal proteína de desecho es la beta-amiloide, cuya acumulación altera el funcionamiento normal de las neuronas.
Reducir el daño en el cerebro
Los investigadores utilizaron modelos de ratón genéticamente programados para producir mayores cantidades de proteína beta-amiloide y desarrollar un deterioro cognitivo significativo similar al alzhéimer. Administraron solo tres dosis de los fármacos supramoleculares y posteriormente monitorizaron regularmente la evolución de la enfermedad.
Solo una hora después de la inyección, observamos una reducción del 50-60 % en la cantidad de beta-amiloide en el cerebro
“Solo una hora después de la inyección, observamos una reducción del 50-60 % en la cantidad de beta-amiloide en el cerebro”, explica Junyang Chen, primer coautor del estudio, investigador del Hospital de China Occidental de la Universidad de Sichuan y estudiante de doctorado del University College de Londres (UCL).
Los datos más impactantes fueron los efectos terapéuticos. Los investigadores realizaron diversos experimentos para analizar el comportamiento de los animales y medir su deterioro de la memoria a lo largo de varios meses, abarcando todas las etapas de la enfermedad. En uno de los experimentos, trataron a un ratón de 12 meses con las nanopartículas y analizaron su comportamiento después de 6 meses. El resultado fue impresionante: el animal, de 18 meses, había recuperado el comportamiento de un ratón sano.
El efecto a largo plazo proviene de la restauración de la vasculatura cerebral, cuyo papel es crucial, especialmente en enfermedades como la demencia y el alzhéimer, donde un sistema vascular comprometido está estrechamente vinculado.
Los autores creen que funciona como una cascada: cuando se acumulan especies tóxicas como la beta-amiloide, la enfermedad progresa. Pero una vez que la vasculatura recupera su función, comienza a eliminar beta-amiloide y otras moléculas dañinas, permitiendo que todo el sistema recupere su equilibrio. Lo notable es que nuestras nanopartículas actúan como un fármaco y parecen activar un mecanismo de retroalimentación que normaliza esta vía de depuración.
Una prueba de concepto
Alberto Rábano, neuropatólogo de la Fundación CIEN, considera el trabajo “muy interesante y muy creíble”, al menos como prueba de concepto en esta fase preclínica de investigación. “Después queda un largo recorrido que va desde aquí al posible desarrollo de nuevos fármacos capaces de modificar la enfermedad humana”, destaca. “Pero está claro que es una nueva vía de abordaje, que tiene especial interés biológico, porque llevamos un tiempo pensando, desde distintos abordajes, que la barrera hematoenecefálica es uno de los elementos claves en la patogenia y en el posible tratamiento del alzhéimer”.
Llevamos un tiempo pensando, desde distintos abordajes, que la barrera hematoenecefálica es uno de los elementos claves en la patogenia y en el posible tratamiento del alzhéimer
Según el experto, se conoce desde hace tiempo que las poblaciones de astrocitos que contribuyen a crear la estructura de la barrera entre el cerebro y el resto del cuerpo se modifican muy significativamente en alzhéimer, y que la posibilidad de modular esa actividad astrocitaria puede ser también clave.
“Ahora, con este otro abordaje, existe la posibilidad de promover a este nivel, el de la barrera, la eliminación de beta-amiloide al compartimento sanguíneo”, comenta Rábano. “¿Será posible trasladar este tratamiento a sujetos humanos sin riesgos significativos? ¿El drenaje de beta-amiloide, composición molecular y dinámica, será suficiente para tener impacto clínico en las fases tempranas de la enfermedad? Esas son las cuestiones que habrá que responder en el desarrollo clínico de esta nueva línea terapéutica”.
Javier S. Burgos, profesor de Farmacología de la Universitat Jaume I, tambiñen considera que es un trabajo muy interesante y que abre nuevas posibilidades de investigación, ya que está dirigida a preservar la integridad de la barrera hematoencefálica, que es un elemento clave que regula el paso de moléculas entre el cerebro y la sangre e impide el paso de sustancias nocivas al sistema nervioso central, y se encuentra comprometida en la enfermedad de Alzheimer.
“No obstante, hay que señalar que el trabajo se ha realizado en un modelo de deposición de placas amiloides en ratones, por lo que tenemos que ser cautos en su traslación a enfermos”, advierte el experto. “Hay que entenderlo como lo que es, una investigación básica que abre puertas muy interesantes en las que seguir trabajando”.





22